
Source : lien:en6q
« La malbouffe n’existe pas ! » C’est à peu près ce que déclarait le Dr Steven N Blair, vice-président du Global Energy Balance Network (GEBN, lien cassé) et professeur au département de Sciences de l’exercice, d’épidémiologie et de statistiques biologiques, School of Public Health (Université de Caroline du Sud aux USA), dans une vidéo (elle aussi supprimée) diffusée par le GEBN.
Son message est simple à résumer : arrêtons de fustiger la consommation de fast food et boissons sucrées à bulles, le secret pour éviter l’obésité est de trouver le juste équilibre (global balance) entre la consommation d’aliments et l’exercice physique. L’obésité, selon lui, est donc un problème de suralimentation (quantité d’aliments) mais pas de nutrition (qualité d’aliments).
Quant aux effets respectifs de l’activité physique et de la nutrition sur le contrôle du poids, ils font l’objet d’une « bataille rangée ». Les défenseurs inconditionnels d’une attention à l’activité physique appuient leur argumentation sur la critique (très pertinente) de la collection et du traitement de données en épidémiologie de la nutrition — voir mon article Faut-il jeter les enquêtes nutritionnelles ?
Des esprits malintentionnés font remarquer que le Professeur Blair n’applique pas ce qu’il enseigne, ou pour le moins que cela ne s’applique pas à son cas personnel (voir photoN1). Quant au journal The Guardian, il s’est fendu d’un article : Nutrition experts alarmed by nonprofit downplaying role of junk food in obesityN2 qui révèle que le GEBN avait été lancé par une donation de 1.5 millions de dollars de Coca Cola® !

Ces turpitudes ont aussi été dénoncées dans un article du New York Times titré Coca-Cola Funds Scientists Who Shift Blame for Obesity Away From Bad DietsN3, suivi d’une lettre adressée aux éditeurs du New York TimesN4 par le Center for Science in the Public Interest et le département de nutrition de Harvard TH Chan School of Public Health, signée par 36 personnalités de la recherche et des cadres de la santé publique, dénonçant que Coca-Cola et ses soutiens académiques n’acceptent pas les preuves bien documentées que les boissons sucrées sont une contribution majeure à l’obésité, aux maladies du cœur, et au diabète.
Après cette levée de boucliers, l’auteur de la vidéo a demandé (le 19 août 2015) qu’elle soit retirée du site du GEBN… Il a exprimé son regret qu’elle ait été utilisée par certains pour laisser croire que le GEBN faisait uniquement la promotion de l’activité physique (sic). En réalité, le GEBN ressemblait plutôt à un espace publicitaire pour la junk food !
Sur une autre vidéo (lien cassé), Steven Blair se plaignait que toute l’activité scientifique se focalise sur l’obésité, alors qu’on ne trouve pas un seul financement — du moins, de ses travaux ! — sur l’exercice physique… A‑t-il jamais utilisé un moteur de recherche ?
Sommaire
⇪ Mise en perspective

Le discours du GEBN, dans sa dimension caricaturale, apparaît comme le recyclage d’une théorie érigée en dogme depuis plusieurs décennies, selon laquelle pour prévenir une prise de poids progressive il suffirait de diminuer l’apport calorique des aliments et/ou d’augmenter la dépense énergétique en faisant de l’exercice physique. Calories positives versus calories négatives, ou le modèle calories-in, calories-out (CICO) pour les anglophones. La qualité serait sans importance… Manger-bouger, vous connaissez ?
Cette équation sonne juste à première vue, bien qu’elle ait été mise en défaut par des travaux en expérimentation animale. Dans son ouvrage FAT — Pourquoi on grossit (2012A2, p. 111 et suivantes), Garry TaubesN6 raconte une expérience de George Wade à l’Université du Massachussets en 1970. Wade étudiait les relations entre les hormones sexuelles, le poids et l’appétit chez des rates ayant subi une ablation des ovaires.
Les effets de l’opération furent assez spectaculaires : les rates se mirent à manger et devinrent rapidement obèses. […] nous étions confortés dans notre opinion selon laquelle, chez la rate comme chez l’être humain, la suralimentation est responsable de l’obésité.
Mais Wade procéda à une seconde expérience de contrôle dont le résultat s’avéra très révélateur : après leur ovariectomie [ablation des ovaires], il soumit certaines rates à un régime post-opératoire strict, ne leur donnant pas plus à manger, malgré leur appétit dévorant, que si elles n’avaient subi aucune intervention. Ce qui se produisit alors n’est pas ce que vous pensez sans doute : les rates en question grossirent autant et aussi vite que les autres. […]
Selon ce que Wade m’a lui-même expliqué, l’animal ne grossit pas parce qu’il mange trop : il mange trop parce qu’il grossit. Nous sommes ici en présence d’une inversion de la cause et de l’effet. Autrement dit, la gloutonnerie et la paresse sont les effets, les conséquences de la prise de graisse : elles sont fondamentalement causées par une anomalie de la régulation du tissu adipeux de l’animal.
Cette citation est suivie d’une explication détaillée du mécanisme de régulation du tissu adipeux dans le contexte de l’intervention sur ces malheureux animaux. Taubes décrit ensuite ces mécanismes chez des animaux ou des humains qui n’ont pas subi d’intervention mais s’adaptent à leur environnement en fonction de leur capital génétique. Il écrit (page 127) :
Dans les années 1950, Jean Mayer étudia dans son laboratoire une de ces lignées de souris obèses. Il rapporta qu’en les affamant suffisamment, il parvenait à faire descendre leur poids au-dessous de celui de souris normales, mais que même ainsi elles « continuaient à présenter plus de graisse que les souris normales alors que leurs muscles avaient fondu ». Ici encore, le problème n’était pas la suralimentation ; comme l’écrivait Mayer, ces souris « transforment en graisse la nourriture qu’elles ingèrent, même dans les conditions les plus défavorables, y compris lorsqu’on les affame à moitié. » […]
Lorsqu’un animal est affamé — et cela vaut également pour l’être humain —, il consomme donc ses muscles pour disposer de carburant, et cela vaut notamment, à terme, pour son muscle cardiaque.
Ce ne sont là que de courts extraits d’un ouvrage de Gary Taubes dont l’argumentation s’appuie sur plusieurs décennies d’expérimentation animale et humaine (voir vidéoN7) mais qui a fait l’objet de critiques véhémentes : voir par exemple le blog The Science of NutritionN8 et la page Big Fat LiesN9. Cela dit, ses contradicteurs, en 2002, agitaient surtout leur chiffon rouge contre la consommation de graisses saturées — voir mon article Pourquoi diminuer le cholestérol ?
➡ L’exposé de Taubes ne résout pas les contradictions d’une surinterprétation des résultats : par exemple, après avoir déclaré que tous les régimes amincissants étaient inefficaces, il fait l’éloge du régime Atkins !
Adam Kosloff a écrit un article (2025N10) traitant de la répartition métabolique des nutriments (metabolic nutrient partitioning) où il critique aussi le modèle calories-in, calories-out (CICO) en citant des expérimentations sur des rats obèses (de Zucker) qui ne perdent pas de graisse même lorsqu’ils sont frappés de sous-nutrition extrême.

Source : N11
Dans son ouvrage The Obesity Epidemic : What caused it ? How can we stop it ? (2015N12), Zoë Harcombe a dénoncé la fallacité d’un calcul basé sur les calories, en raison de la variabilité de l’apport énergétique des nutriments. Elle a fondé sa démonstration sur le deuxième principe de la thermodynamiqueN13 — ce qui me laisse froid, n’ayant pas mis le nez dans un cours de physique théorique depuis une éternité. 😉 Par contre, sur son blog, elle expose, non sans humour, sa tentative d’obtenir des organismes de santé publique au Royaume-Uni une justification scientifique de leur recommandation suivant laquelle un déficit calorique quotidien de 500 Kcal permettrait de « brûler » une livre (454 g) de graisse en une semaineN14. Les articles qui lui ont été signalés en réponse contredisent cette estimation… (Lire aussi les commentaires en bas de page.)

Jane Plain (2014N16) écrit :
S’il s’agissait simplement de calories, on pourrait faire engraisser des gens maigres en les suralimentant. Or on sait bien que les expériences de gavage ratent la plupart du temps. Les maigres ne peuvent pas devenir obèses juste en consommant plus de calories. Cela demande une énorme quantité de nourriture et tout le monde ne profite pas autant, certains résistent totalement.
Bill Lagakos, auteur de The poor, misunderstood calorie (2012A1), résume de manière imagée :
Compter les calories pour perdre du poids ne fonctionne pas pour la majorité des personnes au régime. Cela est dû en partie au fait que les calories contenues dans les aliments ne sont pas les mêmes que celles dépensées par le corps.
Dans une étude publiée en 2015, Fildes et collègues ont suivi jusqu’à 9 années 76 704 hommes et 99 791 femmes obèses (IMC > 30 kg/m2) soignés autrement que par la chirurgie bariatriqueN17. Leur résultat (voir articleN18) :
1283 hommes et 2245 femmes ont atteint leur poids normal. Dans les cas de simple obésité (IMC = 30 à 35 kg/m2), la probabilité chaque année d’atteindre un poids normal était de 1 pour 210 chez les hommes et 1 pour 124 chez les femmes. Elle atteignait 1 pour 1290 pour les hommes et 1 pour 677 chez les femmes à obésité morbide (IMC = 40 à 45 kg/m2). La probabilité chaque année d’une réduction de 5 % du poids était de 1 pour 8 chez les hommes et 1 pour 7 chez les femmes à obésité morbide.
Leur conclusion : Les plans de traitement de l’obésité basés sur des programmes communautaires de gestion du poids sont peut-être inefficaces.
Hélas, les géants de la malbouffe (comme autrefois le lobby du tabac) peuvent continuer à ignorer ces évidences, tant leur discours reste ancré dans la croyance populaire… Il est encore plus regrettable qu’en 2019 des experts français en nutrition humaine (affiliés à l’INRA et l’ANSES) martèlent dans une émission scientifiqueN19 que, pour éliminer le surpoids ou le diabète de type 2N20, il suffirait d’augmenter la dépense énergétique et de réduire l’apport calorique de l’alimentation… Ils ne font que répéter, sans examen critique, une leçon apprise il y a 50 ans ! ? Cela dit, cette émission contenait aussi de nombreux messages clairs, importants et prouvés scientifiquement.
⇪ Tendance dominante
Évitons les jugements à l’emporte-pièce induits par une lecture enthousiaste de Taubes (2012A2) et propagés par celles ou ceux qui « n’arrivent pas à mincir » : diminuer sa ration calorique peut effectivement se traduire dans un premier temps par une perte de poids, perte qui peut être consolidée grâce à une surveillance systématique, par exemple les applications d’évaluation de contenu calorique de tous les repas (Giuily L, 2019N21). Trois problèmes sont liés à cette manière de procéder :
- Cette surveillance fait appel à des algorithmes qui peuvent conduire à un comportement anorexique compensé par de la boulimie chaque fois qu’on « se lâche ».
- Les données traitées par ces algorithmes ne représentent pas la réalité : 100 kilocalories de crème glacée ne produisent pas le même effet à long terme que 100 kcal de haricots ou de viande rouge…
➡ J’utilise l’unité correcte « kilocalories » alors que l’on entend souvent « calories » dans la conversation courante. - Les programmes d’amincissement se soucient uniquement de la perte de poids et non de la santé de l’individu, qui dépend autant de la nature et qualité des aliments que de leur quantité, tout en étant fortement liée à l’activité physique, la réduction du stress, la gestion du sommeil, et — moins connu — les déséquilibres de microbiotes, voir l’article La bouche, miroir de votre santé…

L’efficacité du programme réside donc moins dans le comptage des calories que dans la contrainte qu’il exerce : s’obliger à une surveillance permanente des quantités ingérées. Cette surveillance peut être une planche de salut provisoire chez une personne souffrant de résistance à la leptineN22, l’hormone qui procure la sensation de satiété.
Toutefois, l’échec de cette stratégie sur le long terme (voir le point 3 ci-dessus) s’explique en partie par le fait que la privation de nourriture ne restaure pas « par magie » la sensibilité à la leptine. Il serait plus logique de chercher à retrouver la sensation de satiété, autrement dit manger moins, non par contrainte, mais parce qu’on a moins faim — voir discussion ci-dessous.
Au sujet des pressions exercées par l’industrie agro-alimentaire sur American Society for Nutrition et Academy of Nutrition and Dietetics (aux USA), on lira avec intérêt le rapport de Michele Simon (2015N23) : Nutrition Scientists on the Take from Big Food – Has the American Society for Nutrition lost all credibility ? ainsi qu’un entretien avec l’auteureN24.
Sur la TV américaine, The Biggest Loser est un jeu qui met en compétition des personnes obèses soumises à un régime drastique — Eat Less and Move More — pour perdre du poids. Ils ne reçoivent que 70 % de leurs besoins caloriques et pratiquent chaque jour 90 minutes d’exercice intensif plus de l’entraînement aérobie. Le résultat était spectaculaire : après 30 semaines de ce régime, le poids moyen des candidats en 2015 avait diminué de 149.2 kg à 91.6 kg, ce qui correspondait à une réduction de la masse graisseuse de 49 % à 28 %, sans diminution notable de la masse maigre grâce à l’exercice. Cela paraît miraculeux, sauf qu’après six mois tous les concurrents avaient retrouvé leur poids initial ! Le mécanisme de compensation est expliqué par Jason Fung sur cette pageN25.
La chirurgie bariatriqueN17 présente le même inconvénient, avec un taux d’échec sur le long terme (une dizaine d’années) qui peut avoisiner 40 %. Faute de suivi nutritionnel, les patients risquent de retrouver leurs anciennes habitudes et de s’adonner au grignotage pour absorber plus de nourriture malgré l’obstacle créé par la chirurgie ; et la reprise de poids génère un stress considérable lié au sentiment d’échec.
Sans surprise, l’industrie du médicament, qui contribue largement au financement de la presse médicale, favorise l’opinion selon laquelle, face à l’obésité, tout changement de style de vie est voué à l’échec : c’est une « maladie » qui demande d’être soignée, et non une simple affaire de volonté.
Ce point est discuté en détail par Michael Eades dans The Arrow #155 et The Arrow #156 avec un commentaire de l’essai clinique mené par Louis J Aronne et al. (2023N27) :
C’est le message que vous allez entendre encore et encore. Vous l’entendrez tellement que vous finirez par y croire. Et lorsque vous y croirez, vous pourriez bien vous inscrire pour recevoir des injections hebdomadaires de l’un des nouveaux agonistes du GLP‑1.
Vous vous exposerez alors à un risque accru de pancréatite, de gastroparésie (une sorte de paralysie du tube digestif) et d’obstruction gastro-intestinale. Et peut-être aussi à des épisodes d’idées suicidaires et/ou de dépression.
Si vous êtes comme la personne moyenne qui prend ces médicaments, vous finirez par les arrêter au bout d’un an environ, ce qui est le cas de la plupart des gens. Pourquoi ? Probablement parce que c’est à ce moment-là qu’ils cessent d’agir.
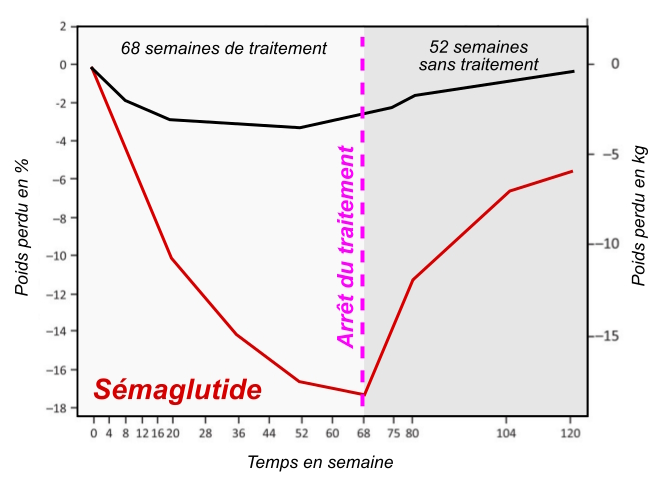
Le graphique ci-dessous montre l’évolution du poids au fil du temps avec le tirzepatide, le plus puissant des nouveaux médicaments injectables pour la perte de poids.
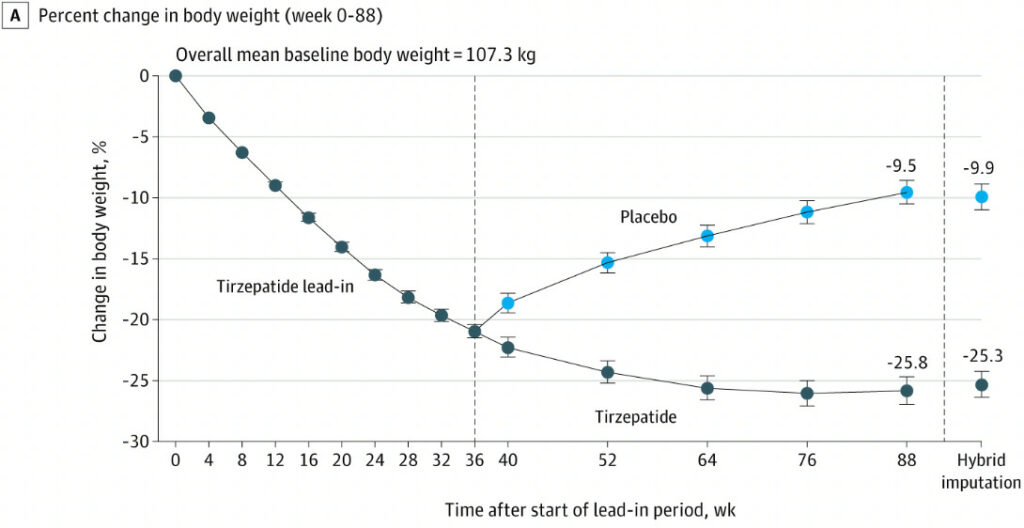
Comme on peut le constater, les personnes qui ont pris un placebo ont fini par reprendre le poids perdu.
Mais regardons d’un peu plus près pour voir ce que nous pouvons tirer d’autre de ce graphique.
Il est assez évident que la perte de poids atteint son point le plus bas lorsque le tirzepatide commence à être administré peu de temps après la randomisation de 36 semaines. Les sujets ayant reçu le traitement complet à base de tirzépatide ont perdu un peu de poids entre la semaine 36 et la semaine 52, mais pas beaucoup. À la semaine 64, ils ont touché le fond et n’ont pas bougé au cours des 24 semaines suivantes.
Il me semble que la courbe commence à remonter, ce qui signifierait que malgré les injections hebdomadaires de tirzepatide, un peu de poids a commencé à revenir. Il est difficile de s’en rendre compte en observant la courbe, mais au moins la perte de poids s’est arrêtée.
Michael Eades aborde, sur la même page, la question de la volonté dans la lutte contre l’obésité. Une partie de son message est traduite dans l’article Prenez le contrôle de votre vie.
⇪ Le modèle glucides-insuline (CIM)
Le modèle défendu par Gary Taubes et ses collègues, en concurrence avec celui de calories-in, calories-out (CICO), s’appelle « glucides-insuline », en anglais Carbohydrate-Insulin Model (CIMN28). Il est associé à un phénomène appelé résistance à l’insulineN29 — voir mon article Insulinorésistance — phase initiale du diabète de type 2N20.
Michael Eades le présente ainsi (The Arrow #111) :
Le modèle glucides-insuline [CIM] postule que les calories entrantes ne sont pas simplement de l’énergie neutre, mais qu’elles provoquent des réponses hormonales métaboliques qui, à leur tour, donnent envie de manger et de stocker des calories. Selon le CIM, les gens ont des degrés variables de tolérance aux glucides, et chez ceux qui y sont intolérants, les glucides provoquent une réponse insulinique plus importante et plus durable. Les niveaux d’insuline continuellement élevés chez ces personnes finissent par entraîner une résistance à l’insuline et une hyperinsulinémie. L’insuline étant l’hormone métabolique qui fait entrer les graisses dans les cellules adipeuses et les y maintient, les personnes qui ont trop d’insuline ont tendance à augmenter leur masse de tissu adipeux.
Lorsque ces personnes mangent, les aliments digérés passent dans le sang, et les centres de l’appétit du cerveau leur signalent qu’elles sont rassasiées. Mais, comme leur taux d’insuline est élevé, les graisses présentes dans le sang sont entraînées rapidement dans les cellules adipeuses, ce qui laisse moins de nutriments dans le sang pour déclencher le signal « assez » dans le cerveau. Au lieu de cela, le cerveau reçoit le signal que les nutriments sont épuisés, et envoie donc le signal de la faim qui donne envie de manger. Ce qui déclenche une sorte de cercle vicieux. Plus de faim = plus d’apport en glucides = plus d’insuline = plus de stockage des graisses = moins d’apport en nutriments dans le sang..
⇪ Compétition entre les modèles
En simplifiant à l’extrême, l’enseignement du modèle CICO serait que, pour perdre du poids, il suffit de diminuer la quantité de calories apportées par l’alimentation et d’augmenter leur utilisation dans l’activité physique. Pour cela, préférer des aliments « moins caloriques ».
Des données physiologiques anciennes — selon Wilber Olin Atwater, qu’on ne discutera pas ici — suggèrent que chaque gramme de glucides fournit en moyenne 4 kcal, contre 4 kcal pour les protéines et 9 kcal pour les graisses. Il s’ensuit qu’un régime « hypocalorique » se doit d’éliminer les graisses au profit des glucides — en anglais low-fat high-carb (LFHC).
À l’inverse, selon le même mode simpliste de raisonnement, le modèle CIM préconiserait de diminuer l’apport en glucides qui ont pour effet d’augmenter le tax d’insuline et d’induire une résistance à l’insulineN29. D’où la préférence pour un régime faible en glucides, en anglais low-carb high-fat (LCHF).
La bataille entre ces deux écoles est féroce. Elle a donné lieu à de nombreux essais cliniques randomisés (Public Health Collaboration, 2024N30), difficiles à conduire car il faut pour cela comparer les deux régimes avec le même apport calorique alimentaire et la même dépense énergétique.
La définition de chaque régime est elle-même un facteur de confusion : par exemple, la notion de « faible en glucides » peut s’étendre à une diète cétogèneN31 — voir mon article Diète cétogène – expérience — ou à un régime carnivore — voir mon article Carnivore Code.
⇪ Une « troisième voie »
La compétition entre les modèles CICO et CIM est résumée dans une conférence de Dr Michael Eades (2023N32), qui suggère une troisième alternative. Il constate, en effet, que la formule « CICO » (calories in moins calories out) exprime une différence d’énergie, alors que ce qu’attendrait une personne obèse est une différence de poids (ou de masses). Il serait donc préférable de chercher à diminuer la quantité masse en entrée moins masse en sortie.
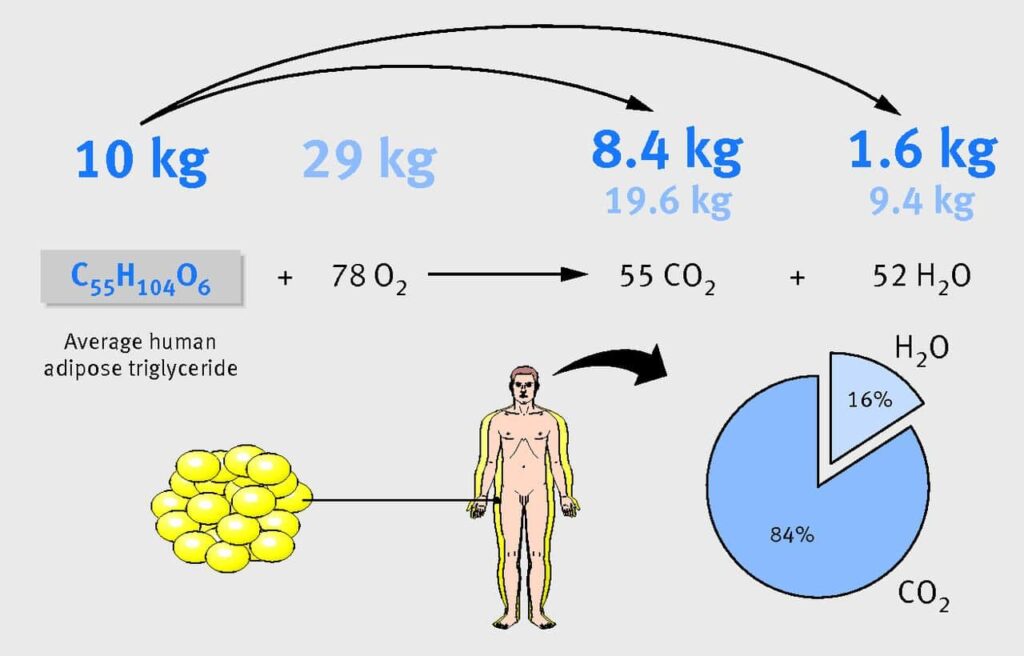
La masse en entrée est celle des aliments ingérés. La masse en sortie est ce que nous éliminons. Or l’oxydation des graisses produit du gaz carbonique et de l’eau.
Exemple pour un triglycéride adipeux humain :
C55H10406 + 78 O2 –> 55 CO2 + 52 H2O
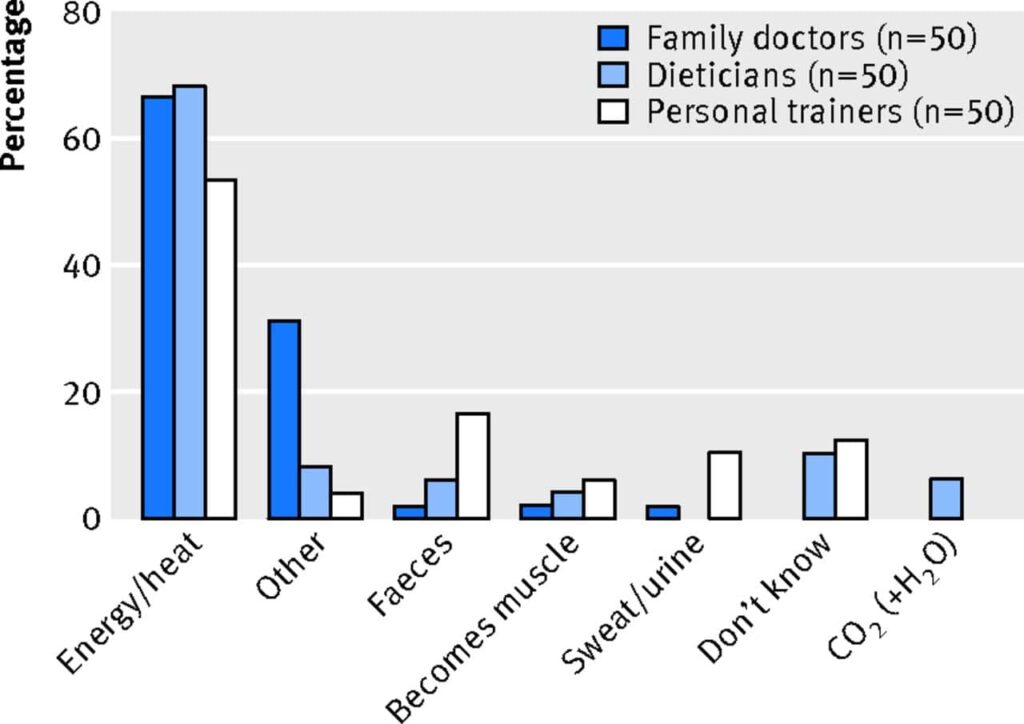
Dans son article Quand quelqu’un perd du poids, où va la graisse ?, Ruben Meerman montre que — contrairement aux croyances d’une majorité de professionnels de santé — « les poumons sont le principal organe excréteur de la perte de poids [84 % en masse], [les 16 %] d’eau formée pouvant être excrétés dans l’urine, les fèces, la sueur, l’haleine, les larmes ou d’autres fluides corporels » (Meerman R, 2014N33).
Eades cite un passage en vidéo (2023N32 24:06) où Meerman soufflait dans un ballon qu’il refroidissait ensuite avec de l’azote liquide, ce qui avait pour effet de liquéfier l’oxygène restant et de solidifier le gaz carbonique, les rendant visibles :
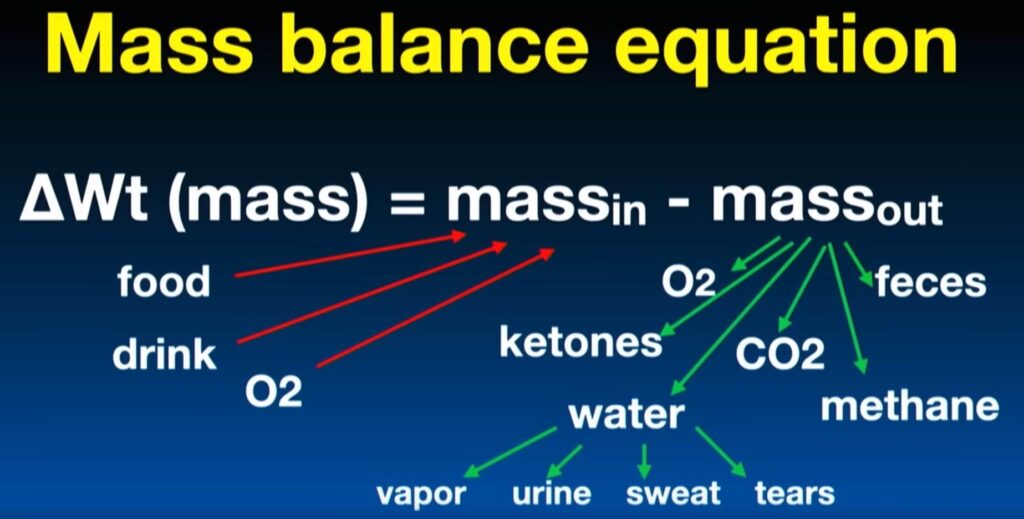
Pour perdre du poids, il faudrait donc logiquement diminuer la masse en entrée plutôt que la quantité d’énergie. C’est une équation de conservation de la masse qui est en jeu, et non de conservation d’énergie. Sachant que les individus ont tendance naturellement à ajuster leur consommation d’énergie — leurs « calories » — à leur activité, il convient donc, pour perdre du poids, d’accorder la préférence aux « calories légères » — celles des graisses — plutôt qu’aux « calories lourdes », celles des glucides.

Michael Eades donne une idée de la différence de masses en entrée entre un régime low-carb high-fat (LCHF) et un low-fat high-carb (LFHC), tous deux calibrés à 2500 kcal/jour (2023N32 36:35). Le premier serait plus « léger » de 157 grammes — ce qui reflète, selon lui, la moyenne de perte de poids quotidienne lorsque ce régime est effectivement pratiqué.
Cette simple démonstration prêche donc en faveur des régimes LCHF sans besoin de s’appuyer sur le modèle CIM. C’est pourquoi elle a été présentée par Michael Eades comme une « troisième voie » (The Arrow #111) :
[…] je pense que les personnes qui suivent un régime pauvre en glucides reçoivent une double dose de bienfaits. Limiter les glucides réduit la masse dont il faut se débarrasser, ce qui est la première étape. Et limiter les glucides réduit également la quantité d’insuline produite, ce qui, à terme, permet de se débarrasser de la résistance à l’insuline et de l’hyperinsulinémie.
Par conséquent, la graisse peut facilement sortir des cellules adipeuses et fournir de l’énergie, au lieu d’être piégée, ce qui signale au cerveau qu’il y a beaucoup de nourriture à bord. Le cerveau réduit la faim, de sorte qu’il n’y a pas de forte compulsion à manger. C’est tout le contraire du cercle vicieux du « manger moins, bouger plus », c’est un cycle bénéfique.
Cette explication évoque en filigrane d’autres phénomènes impliqués dans la prise ou la réduction du poids, notamment le rôle de la leptineN34 en tant qu’hormone de « signalement de la satiété », voir plus bas.
⇪ Exercice
Dans l’expérience The Biggest Loser, l’accent était mis sur la nutrition, qui n’est qu’un des deux termes de l’équation nutrition/exercice. Or « faire de l’exercice » ne va pas de soi. La même dépense physique ne produit pas les mêmes effets sur la santé (et donc le poids) selon qu’on pratique un sport, du jardinage, de la randonnée etc.
Cette distinction est exposée en détail dans les pages consacrées à L'exercice sur ce site. Pour faciliter l’élimination du surpoids grâce à une amélioration de sa forme physique, il est indispensable de mettre en place une pratique quotidienne (voire bi-quotidienne) d’exercice d'endurance (« cardio »). Mais il est surtout vital d’en « calibrer » l’intensité, à n’importe quel âge et n’importe quel niveau d’entraînement, afin d’éviter un sous-entraînement inefficace, ou un surentraînement qui mettrait en danger le système cardiovasculaire.
Le meilleur calibrage d’intensité, à ma connaissance, sans recours à un appareillage coûteux et compliqué, consiste à maintenir son rythme cardiaque à la valeur optimale calculée selon les recommandationsN35 du Dr Philip Maffetone : la formule « 180 – votre âge » — soit par exemple 130 bpm pour une personne âgée de 50 ans. Formule à ajuster en fonction de critères de santé et de pratique d’entraînement.
Sur un vélo d’appartement — ou une autre machine comme le vélo elliptique — on peut mesurer l’énergie dépensée et la rapporter à la durée de l’exercice : par exemple 300 Kcal en 27 minutes. Noter au passage que cette « perte énergétique » serait compensée par la consommation de 75 grammes de glucides ou 38 grammes de graisse, disons une tartine beurrée à la confiture ! Les variations de ce rapport 300/27 — dans des circonstances identiques — nous renseignent sur l’augmentation de la forme physique, ou au contraire une diminution qui peut signaler, soit un entraînement à un rythme cardiaque excessif, soit une détérioration de la santé à prendre en charge médicalement.
Avec ce calibrage, une personne en surpoids se mettra certainement à transpirer avant la fin de chaque séance. Un bon indice pour en fixer la durée minimale est de suer à grosses gouttes au moins pendant une dizaine de minutes. Cela peut correspondre (en ordre de grandeur) à deux séances de 30 minutes chaque jour, nettement plus efficaces que l’heure de promenade, de jardinage, ou toute autre activité « sportive » prescrite par des soignants qui n’ont jamais été confrontés à l’obésité. Rien ne s’oppose à ce qu’on meuble ce temps par l’écoute de podcasts, la radio ou la TV, l’apprentissage d’une langue étrangère, etc., avec un œil sur le cardiofréquencemètre, et sous condition que l’activité de divertissement ne perturbe pas la fréquence cardiaque — donc éviter certaines musiques ! La fiabilité de l’instrument de mesure est vitale, voir mon article Exercice d'endurance.
La masse musculaire est le plus volumineux organe de notre corps. Cet organe est en charge de bien d’autres fonctions que l’équilibre postural et la mobilité. Sa réduction peut être masquée par l’accumulation de graisse (obésité sarcopénique) — voir mon article Vivre bien et longtemps. L’exercice d’endurance n’est pas suffisant pour son entretien. Il doit être complété par de l’exercice « contre résistance » — une forme de musculation que l’on peut pratiquer sous la forme d’entraînement fractionné de haute intensité (HIIT) ou/et, plus simplement, d’entraînement musculaire MAF.
C’est en intégrant à la vie quotidienne ces formes de pratique qu’on peut évaluer — pour soi — la véritable incidence de l’activité physique sur le maintien en bonne santé, la maîtrise du poids et l’entretien de la masse musculaire.
Dans une vidéo en apparence provocatrice (2021N36), l’entraîneur sportif (et ancien athlète) Mark Sisson déclare que « faire de l’exercice est une mauvaise méthode pour perdre du poids »… Il expose les mêmes arguments qu’au début de cet article, notamment que toute dépense calorique supplémentaire en exercice sera compensée par un supplément de prise alimentaire, mais aussi par l’économie d’adaptations métaboliques vitales, comme la réparation de tissus défectueux, la menstruation etc.
Il est important de faire une distinction claire entre les objectifs « perdre du poids » et « augmenter la masse musculaire ». Les deux sont souvent contradictoires. Georgi Dinkov a montré l’intérêt d’augmenter le rapport entre masse musculaire et masse grasse, pour limiter la production de cortisol (voir plus bas) qui est une source d’inflammation systémique — voir le paragraphe Mise en garde sur le métabolisme des graisses.
Une des solutions proposées par Mark Sisson est la construction d’un style de vie (qu’il appelle « primal ») plus proche de celui de nos ancêtres, caractérisé par une moindre consommation de glucides, et des périodes de restriction calorique alternant avec celles d’abondance — le principe du demi-jeûne fractionné présenté sur mon article Jeûne et restriction calorique.
Le mécanisme de l’adaptation métabolique à la perte de poids est exposé plus en détail dans un autre exposé en français (Thai J, 2021N37). Cet auteur y constate qu’après une période d’amincissement liée à un régime et une forte dépense calorique, l’augmentation progressive de l’apport calorique — pour restituer la balance énergétique — peut induire une reprise plus rapide du poids perdu si les aliments sont trop savoureux. Toutefois, à l’inverse de « vieux routards » comme Mark Sisson et Philip Maffetone, cet entraîneur appuie son exposé sur des travaux de portée scientifique limitée : expérimentation sur de très petits groupes de (jeunes) sujets, et sur des durées dépassant rarement quelques semaines. Les résultats visent donc les performances sportives plutôt que l’état de santé sur le long terme.
⇪ Thermogenèse
Un autre mécanisme de régulation du poids pourrait être la thermogenèse due à l’activité autre que l’exercice (NEAT, nonexercise activity thermogenesis), autrement dit tous les mouvements que nous exécutons spontanément durant la journée sans les avoir programmés en tant qu’exercice. Cette activité augmente avec la quantité de masse graisseuse (Villablanca PA et al., 2015N38). Mais plus on s’agite volontairement, plus on a tendance involontairement à réduire l’activité NEAT, ce qui expliquerait en partie le manque d’efficacité de l’exercice.
La thermogenèse est une des fonctions spécifiques de la graisse brune (tissu adipeux brunN39) qui intervient aussi dans la régulation du poids par l’élimination de triglycéridesN40 entraînant une diminution de la graisse blanche. Contrairement aux adipocytes blancs qui contiennent une gouttelette lipidique unique, les adipocytes bruns contiennent de nombreuses gouttelettes plus petites et un nombre beaucoup plus élevé de mitochondries qui contiennent du fer, donnant au tissu sa couleur bruneN39. Des travaux récents (Cypess AM et al., 2009N41) ont montré que cette graisse brune n’était pas fonctionnelle que sur les sujets jeunes, mais potentiellement aussi chez les adultes, surtout les femmes, ainsi que les personnes âgées. La graisse brune est aussi productrice de leptineN34 qui a pour effet de diminuer l’appétit (voir plus bas).
Certains auteurs affirment que l’on peut relancer ou entretenir l’activité de la graisse brune par l’exposition régulière à des douches froides, voire l’application répétée de glace ou l’ingestion de 500 ml d’eau glacée le matin (Ice therapy de Tim Ferriss). Il n’est pas certain que ces recettes conviennent à tous les individus et tous les âges, mais on peut toujours essayer…
⇪ Microbiotes
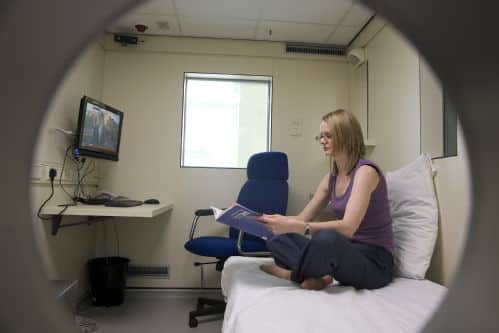
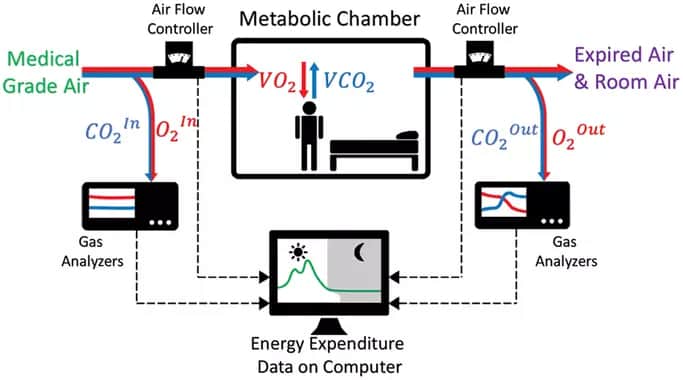
Le microbiote intestinalN42 joue certainement un rôle essentiel dans la régulation du poids, bien qu’il soit très difficile à caractériser, car très variable selon les individus, leurs âges et conditions de vie. L’étude de cette flore bactérienne est complexe en raison de sa diversité que l’on commence à caractériser à l’aide de techniques nouvelles, comme le séquençage ADN à haut débit.
L’analyse des gaz respiratoires permet toutefois de détecter des dysbiosesN43 et de corriger en conséquence le régime alimentaire. Les microbiotes du côlon et des différentes parties de l’intestin grêle, très différents, sont à prendre en compte, ainsi que ceux de l’estomac et de la bouche. L’examen buccal permet de rendre visibles, par luminescence, les bactéries colonisatrices (Holef C, 2021N44). Voir à ce sujet les travaux du Dr Bruno Donatini, présentés sur mon article La bouche, miroir de notre santé.
Les probiotiquesN45 et prébiotiquesN46 agissent sur cette flore, mais ce n’est pas sans conséquence, car certains probiotiques peuvent aussi contribuer à une prise de poidsN47. L’abstinence de yaourt pendant la période d’amincissement — telle que prescrite en chrono-nutrition®N48 — serait donc une saine précaution à étendre à d’autres probiotiques.
Renaud Roussel, préparateur physique et nutritionniste, partageait sur Facebook (28 octobre 2022) :
L’activité physique a de multiples vertus, mais pas celle de faire perdre du poids.
Je connais des marathoniens qui prennent du poids inexorablement !
Peu importe l’apport calorique, c’est la nature de l’aliment qui compte.
Les sucres fermentescibles stimulent la flore [bactérienne] qui produit une graisse (céramidesN49 circulants) presque indestructible par nos lysosomes, inutilisable par nos mitochondries, et intouchable par notre autophagie.
Couper la source de cette production de graisse : les sucres fermentescibles, permet de réduire la flore de fermentation coupable de la prise de poids.
Réintroduire une bonne flore, concurrente de la flore de fermentation, permet de stimuler les gènes de l’autophagie, et la destruction des graisses problématiques et inflammatoires.
A cette condition, l’activité physique aidera à utiliser les graisses stockées et accumulées.
La perte de poids pérenne est une histoire de métabolisme, pas de balance calorique.
⇪ Stress
L’influence du stress sur le stockage de la masse graisseuse est aussi un des facteurs bien connus à prendre en considération :
Quand l’organisme est contraint de produire adrénaline et cortisol jour après jour, le corps doit renouveler constamment ses réserves d’énergie. Il en emmagasine donc, sous forme de tissus adipeux, autour de la taille. C’est une solution pratique, car le cortisol sécrété par les glandes surrénales, situées au-dessus des reins, y a ainsi facilement accès. Au besoin, il puisera dans ces graisses pour les transformer en sucre.
(Le rôle du cortisol dans l’excès de poids et l’embonpointN50)
Un excès de cortisol chronique peut se traduire par une maladie endocrinienne appelée syndrome de Cushing. Selon WikipediaN51 : La manifestation la plus visible chez l’homme est l’apparition d’une obésité chronique de la partie supérieure du corps, un aspect bouffi du visage, des manifestations cutanées et un hirsutisme, ainsi que des troubles psychologiques variés.
⇪ Carences diverses
La correction d’un déséquilibre nutritionnel exige d’améliorer à la fois le choix des aliments et leur qualité. En effet, les fruits et légumes, viandes et laitages issus de l’industrie agroalimentaire sont issus de sols appauvris par les engrais ou d’animaux en déséquilibre nutritionnel. Une supplémentation en vitamines synthétiques est sans effet si d’autres micronutriments sont en quantité insuffisante : magnésium, potassium, vitamines E et K, antioxydants, etc.
Dans un éditorial du 16 janvier 2016N52, le journal The Lancet conclut :
Bien que les stratégies nationales de lutte contre l’obésité soient bienvenues et très demandées, il faut qu’elles soient bien orchestrées en impliquant toutes les instances gouvernementales concernées et en couvrant à la fois la prévention et le traitement. En plus du secteur de la santé, celui de l’éducation joue un rôle vital en permettant l’autonomisation des enfants et des adolescents, grâce à des connaissances pertinentes sur les aliments et la nutrition, ainsi que la possibilité de faire de l’exercice au-delà de la compétition sportive. Les ministères du transport et de l’urbanisme doivent veiller à ce que les villes et les environnements facilitent et privilégient l’accès à une alimentation saine et à l’activité physique.
Les ministères de l’économie et les entreprises ont besoin d’être tenus pour responsables des effets sur la santé de leurs politiques. Lutter contre l’obésité chez les enfants et les adultes est difficile. Les stratégies de traitement sont multiples, et commencent par la nécessité de reconnaître le surpoids et l’obésité et leurs conséquences, allant de l’information et des conseils nutritionnels à la chirurgie bariatriqueN17. Les interventions face à l’obésité infantile ne fonctionnent que si toute la famille est impliquée. Toute stratégie nationale devrait avoir des indications claires sur le traitement de l’obésité et du surpoids qualifiés.
L’obésité est une forme de malnutrition grave. Le rapport scientifique du Comité consultatif des 2015 Dietary GuidelinesN53 indique que la population des États-Unis a un déficit de nutriments essentiels, tels que les vitamines A, D, E et C, d’acide folique, de calcium, de magnésium, de fibres, de potassium et de fer. Si les deux tiers de la population avaient de graves dénutritions ou de l’anorexie mentale, il y aurait une urgence nationale reconnue.
L’obésité nécessite une attention beaucoup plus forte que celle que lui accordent actuellement les pays et organisations mondiales de santé. L’objectif de réduction de sucre par l’introduction d’une taxe sur le sucre est un petit pas dans la bonne direction. Néanmoins, il ne doit pas nous détourner de la nécessité de mesures bien plus profondes à plus large échelle.
⇪ Nouvelles pistes
Une étude publiée dans Nature par Andrew J Whittle et al. (2015N54) révèle un mécanisme d’accumulation qui confirme l’inefficacité de la seule pratique de réduction calorique pour contrer l’obésité (voir article en anglaisN55). Les cellules adipeuses fabriquent une protéine (sLR11) qui inhibe la dissipation d’énergie accumulée sous forme de chaleur (thermogenèseN56). Les individus chez qui la production de sLR11 est faible peuvent réguler leur poids, alors que ceux qui ont une forte production tendent à maintenir l’énergie stockée sous forme de graisse.
La chirurgie bariatriqueN17, en réduisant la masse graisseuse, peut contribuer à diminuer la quantité de sLR11, ce qui se traduirait par une meilleure régulation du poids. Des effets secondaires doivent toutefois être pris en considération (Mandal A, 2019N57 ; article en français, 2020N58). Son indication actuelle est un indice de masse corporelle supérieur à 40 kg/m2, ou 35 kg/m2 avec des comorbidités associées.
L’équipe de Thoams Thomou et al. (2017N59) a observé sur un modèle animal que les cellules adipeuses envoyaient des « messagers » (miRNAs) modifiant l’expression de gènes et la production de protéines dans l’organisme. Certains s’assemblent en paquets (exomesN60) dans le sang. Un taux sanguin élevé de miRNAs serait associé à l’obésité, au diabète et à des maladies cardiovasculaires. En injectant de la graisse brune à des souris génétiquement modifiées pour produire un faible taux de miRNAs, ils ont observé que le mécanisme du glucose revenait à la normaleN61. Dans une autre expérience, ils ont montré que le miRNA communique avec le foie et régule l’expression de gènes (comme Fgf21). Pour résumer, les cellules adipeuses peuvent « communiquer » avec les organes pour modifier la tolérance au glucose.
Ces découvertes permettent d’entrevoir une approche nouvelle de la lutte médicamenteuse contre l’obésité, mais aussi, par la maîtrise du mécanisme inverse, de moyens d’augmenter le stockage de graisse chez ceux qui souffrent d’anorexie nerveuseN62.
Sur la page The Carbohydrate Hypothesis of Obesity : a Critical ExaminationN63, Stephan Guyenet remet en cause l’hypothèse — popularisée par Gary Taubes (2024N64 p. 62-ff) et une majorité de chercheurs — que l’élévation du taux d’insuline serait la cause première de l’obésité. Il affirme que cette hypothèse n’est pas validée expérimentalement, et que, entre autres, l’augmentation de poids chez des patients diabétiques traités à l’insuline pourrait avoir d’autres causes que l’insuline elle-même.
Les obèses n’ont pas une incapacité à libérer de la graisse de leurs cellules adipeuses et à la brûler, au contraire. Ils libèrent plus de graisse de leurs cellules adipeuses que les gens minces, et en brûlent plus. Mais ce ce processus est compensé par une plus grande absorption d’énergie, et un taux plus élevé d’absorption de la graisse dans les cellules adipeuses qui contrebalance la dépense accrue… Pour comprendre l’obésité, il nous faut comprendre ce qui cause l’augmentation de prise de nourriture, et ce n’est pas l’insuline.
Les études font apparaître notamment des facteurs génétiques qui prédisposent le système nerveux central à consommer plus de nourriture. Toujours selon Guyenet,
Parmi les nombreux types de gènes identifiés comme associés à une variabilité de l’indice de masse corporelle, et dont la fonction est connue, la grande majorité s’expriment dans le cerveau, particulièrement l’hypothalamus, et certains concernent le mécanisme de signalement de la leptineN34 (41N65, 42N66).
La leptine est une hormone qui induit dans le cerveau une sensation de satiété — voir Hic & Nunc (2015N67) et Gabriella Tamas (2020N22). Elle est elle-même produite par les cellules adipeuses en réponse au stockage de graisse. Elle intervient dans les processus de l’absorption intestinale, de la signalisation de la satiété, de la lipolyse, de l’angiogenèse, de la reproduction et des réponses inflammatoiresN22. Un excès de production peut entraîner une insensibilité à la leptine, une cause d’obésité que l’on ne peut régler qu’en modifiant son alimentation.
Sur la même page (2011N63), Guyenet montre que l’index insulinogénique (prédisant l’élévation du taux d’insuline associée à la prise d’un aliment) ne suffit pas à expliquer que les sucres raffinés provoquent plus d’obésité que les sucres naturels, alors que leurs index peuvent être identiques, et encore moins que certains régimes riches en protéines favorisent la perte de poids.
Des aliments riches en protéines, comme la viande de bœuf, peuvent accroître la sécrétion d’insuline autant que certains aliments amidonnés comme les pâtes, et même plus. Les régimes riches en protéines, comme beaucoup d’entre vous le savent, aident à perdre du poids. Certains auteurs ont suggéré que c’était en raison de la sécrétation de glucagonN68 par le pancréas en réponse aux protéines. Cela peut très bien jouer un rôle, mais si nous parlons de glucagon, alors pourquoi ne pas reconnaître l’influence d’autres signaux, mise à part l’insuline, dans ce processus ? C’est le point de vue plus vaste que je cherche à promouvoir ici : on ne peut pas regarder uniquement l’insuline, il faut aussi prendre en compte l’amylineN69, le glucagonN68, le GLP‑1N70, la ghrélineN71, la leptineN34, la dilatation de l’estomac, et tous les autres signaux à court et long terme activés en réponse à l’ingestion de nutriments et aux changements de masse grasse corporelle. Ces signaux règlent collectivement la prise de nourriture et la corpulence à long terme via le cerveau.
L’auteur cite enfin de nombreux cas de populations dont la nourriture était proportionnellement riche en glucides alors que l’obésité leur était inconnue. Il conclut :
La consommation de glucides, en soi, n’est pas la cause de l’épidémie d’obésité. Toutefois, lorsque l’obésité ou l’excès de poids sont établis, la restriction des glucides peut aider la perte de poids chez certaines personnes. Le mécanisme impliqué n’est pas très clair, mais il n’y a pas de preuve que l’insuline joue un rôle principal dans ce processus. La restriction des glucides diminue automatiquement l’absorption de calories (de même que, à moindre effet, la restriction des graisses), ce qui suggère qu’elle modifierait l’homéostasieN72 de la graisse corporelle, mais il n’y a pas de preuve convaincante que cela arrive en raison d’une influence hormonale directe sur les tissus adipeux. Le cerveau est le principal régulateur homéostatique de la masse graisseuse, de même qu’il régule homéostatiquement la pression sanguine, le rythme respiratoire et la température corporelle.
Une discussion approfondie de cette proposition — régulation de la masse graisseuse par le cerveau — est présentée sur cette page : Testing the Insulin Model : A Response to Dr Ludwig (2016N73). Le mécanisme décrit par Guyenet et Schwartz (2012N74) est illustré ci-dessous. La leptineN34 apparaîtrait comme un important agent régulateur dans ce processus.
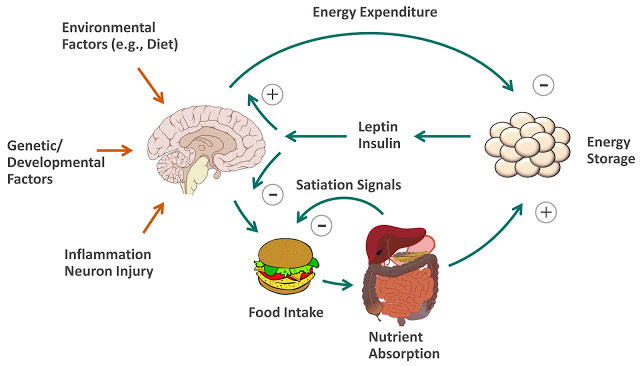
Les modèles de Guyenet et de Taubes sont moins antagonistes que le laissent paraître les échanges d’arguments (exemple en 2011N75). Robert Lustig a en effet montré (AHS11, 2011N76) que l’hyperinsulinismeN77 provoquerait de la résistance à la leptineN34, ce qui a pour effet une accumulation des facteurs de prise de poids. D’autre part, bien que l’insuline produise à court terme une sensation de satiété, l’hyperinsulinisme est marqué sur le long terme par une augmentation de l’appétit (Eenfeldt A, 2011N78).
Le rôle majeur de l’insuline dans la prise de poids a été réaffirmé par Nicole M Templeman et al. (2017N79), apportant « de nouvelles preuves démontrant que des réductions modérées de l’insuline circulante empêchent le gain de poids, avec des effets soutenus qui peuvent persister après normalisation des niveaux d’insuline ».
Toutefois, l’action directe de l’insuline induisant le stockage de graisses dans les cellules adipeuses ne suffit pas, à elle seule, à expliquer la prise de poids (Speakman JR & KD Hall, 2021N80) :
La cause première de l’obésité humaine courante reste incertaine. Il existe plusieurs explications plausibles, dont le modèle populaire « glucides-insuline » (CIM), qui suggère que la prise de graisse corporelle résulte de la consommation de glucides qui stimulent l’insuline postprandiale, ce qui favorise le stockage d’énergie et la poursuite de l’ingestion dans un cercle vicieux. La base théorique de la CIM a été réfutée par plusieurs expériences récentes. Nous suggérons que, bien que l’insuline joue un rôle important dans la régulation de la graisse corporelle, la CIM échoue parce qu’elle se concentre sur l’action directe de l’insuline sur le tissu adipeux après la consommation d’un repas contenant des glucides. Nous proposons plutôt de mieux comprendre le rôle de l’insuline dans l’obésité en tenant compte de son action pléiotropiqueN81 sur de multiples organes, qui est déterminée par des facteurs essentiellement indépendants de la consommation de glucides. Reconsidérer le rôle de l’insuline peut améliorer notre compréhension des causes de l’obésité et de son traitement.
Jane Plain écrit à ce sujet (voir N16) :
Si vous suivez un régime alimentaire pour réduire votre tissu adipeux et le diamètre des cellules adipocytes en utilisant plus de matières grasses en tant qu’énergie… autrement dit, vous privez votre tissu gras d’un signal correct d’insuline… ce qui se passe est que vos adipocytes rétrécissent. En réponse à cet écoulement de graisse des adipocytes, sans que l’insuline puisse y mettre fin en induisant du stockage, la synthèse de la leptine [N34] s’arrête, et elle s’arrête de manière bien plus spectaculaire que votre niveau absolu de de masse grasse. En outre, les [protéines] réceptrices de la leptine augmentent, emprisonnant la leptine dans le sang et la rendant inactive [voirN82]. Dans le fonctionnement normal de 100 % des régimes amincissants basés sur la nourriture ou un changement de comportement, la leptine diminue et les récepteurs qui emprisonnent la leptine augmentent. Cela fait partie intégrante DE TOUTES LES PERTES DE POIDS PROVOQUÉES PAR DES RÉGIMES OU DE L’EXERCICE.
[…] Le résultat est que les hommes perdent leur libido, les femmes cessent d’ovuler ou sautent des cycles, vous avez froid, vous vous sentez fatigué, vous devenez obsédé par la nourriture et vous voulez manger tout le temps, et vous ne vous sentez jamais énergique. La consommation de carburant au niveau cellulaire est altérée.
[…] Tous ces « trucs » ne fonctionnent que par un abaissement supplémentaire du glucose et de l’insuline sur une période de 24 heures. Oui, la perte de poids se produit, mais non, elle ne corrige pas ou n’empêche pas un état de famine, elle l’aggrave en réalité. Il n’y a aucun moyen de dissocier la chaîne insuline/glucose/croissance de graisse/leptine. UNIQUEMENT DES INJECTIONS DE LEPTINE POURRAIENT Y REMÉDIER.
[…] Il est bien établi que la graisse du corps est sous le contrôle de la leptine par l’intermédiaire des effets centraux et périphériques. Il n’y a pas de régime magique qui permette un contrôle du poids sans effort. Voilà pourquoi la plupart des gourous “low carb” de l’alimentation sont en surpoids, obèses, ou n’ont jamais eu de graisse en premier lieu.
Le rôle de la leptineN34 est mis en avant dans une maladie congénitale rare associée à un syndrome de lipodystrophieN83 (Huang-Doran I et al., 2010N84) dans laquelle les tissus adipeux ne stockent pas de graisse, de sorte que les personnes sont très minces alors que par ailleurs elles consomment beaucoup de nourriture et présentent les symptômes de personnes gravement obèses : hyperinsulinismeN77, stéatose hépatique non-alcooliqueN85, hypertension, hypercholestérolémieN86 que l’on regroupe sous le qualificatif de syndrome métaboliqueN87 (Kolata G, 2016N88). En expérimentation animale, un apport artificiel de graisse fait disparaître ces symptômes, en restaurant la fabrication de leptine qui envoie au cerveau les signaux de satiété.
À l’opposé, 10 à 20 % de personnes obèses ne développent aucun signe de syndrome métabolique (Frabbrini E et al., 2015N89)… Indépendamment de ces cas, plusieurs études convergent vers ce qu’on appelle le paradoxe de l’obésité : selon la méta-analyse de Katherine M Flegal et al. (2013N90), les personnes faiblement obèses (IMC de 30 à 35) n’auraient pas un risque accru de mortalité par diverses maladies, et celles en surpoids (IMC de 25 à 30) auraient même un risque diminué par rapport aux personnes plus minces. Ce résultat est confirmé par Heather M Orpana et al. (2012N91) qui ont suivi plus de 11 000 personnes à partir de 1994–1995 au Canada.
Toutefois, ce paradoxe est contredit par une autre méta-analyse couvrant plus de 30 millions de sujets (Dagfinn A et al., 2016N92). Stephan Guyenet (2016N93) souligne qu’il a suffi pour cela d’éliminer deux facteurs confondants : (1) les personnes malades ont tendance à maigrir et (2) les fumeurs sont généralement plus minces. D’autre part, les personnes souffrant de maladies cardiovasculaires ont intérêt à maîtriser leur poids (Dorner TE & A Rieder, 2012N94).
Dans un article qui résume bien les mécanismes en jeu, Roger H Unger et Philipp E Scherer (2010N95) écrivent :
[…] l’obésité en soi ne peut pas et ne doit pas être associée au syndrome métaboliqueN87. Il est reconnu depuis de nombreuses années qu’il existe une corrélation positive entre la taille des dépôts adipeux et la sensibilité à l’insuline, si l’emplacement de la matière grasse est pris en considération.
[…] La plupart des coussinets adipeux de protection sont ceux qui subissent un processus d’expansion « sain ». Nous définissons un coussinet de graisse saine comme celui qui a un plus grand nombre de cellules graisseuses plus petites, est bien vasculariséN96 et peu fibrosantN97, et qui par conséquent affiche un niveau réduit de nécroseN98 locale des tissus adipeux, [celle-ci étant] souvent associée à un haut degré d’inflammation locale (et, finalement, systémique). La possibilité d’étendre le tissu adipeux de manière protectrice est clairement déterminée génétiquement, et a aussi une forte composante dimorphique sexuelle.
Les femmes, quel que soit leur indice de masse corporelleN99, sont mieux protégés que les hommes contre la résistance à l’insuline.
⇪ Se serrer la ceinture…

Le lien (ou l’absence de lien) entre obésité et syndrome métaboliqueN87 apparaît plus clairement avec la distinction entre graisse sous-cutanée et graisse viscérale (principalement abdominale). Autrement dit, c’est le tour de taille qui est à surveiller, plus que le poids ou l’indice de masse corporelle…
La graisse stockée en superficie sous la peau est une simple réserve d’énergie, de taille variable selon les individus. Par contre, une fois cette capacité de stockage saturée, la graisse s’accumule dans l’abdomen — autour des viscères. Or ce lieu n’est pas conçu pour le stockage de graisse.
L’organisme réagit donc contre cette invasion de matières qui entravent le fonctionnement des organes. Comme à l’intérieur d’une plaie infectée, cette réaction immunitaire se traduit par la production de macrophagesN100 qui stimulent la formation de cytokinesN101 pour attaquer ce corps étranger. La masse totale des macrophages peut avoisiner celle de la graisse viscérale. C’est ce milieu qui est favorable à l’apparition de maladies qu’on associe au syndrome métabolique : résistance à l’insuline, diabète de type 2, maladies cardiovasculaires, cancers, etc.

Cette obésité (abdominale) peut donc être désignée comme une pathologie, malgré que ce discours soit en rupture avec l’injonction de ne pas stigmatiser une personne en surpoids — « obèse » étant aujourd’hui perçu comme une insulte « grossophobe ». Pour avoir vécu plusieurs décennies dans l’inconfort de l’obésité, j’ai gardé le souvenir du regard apitoyé ou moqueur des personnes « bien portantes ». Mais le déni — syndrome d’Obélix — ne permet pas d’échapper à la haine de soi…
La bonne nouvelle est qu’une révision des habitudes nutritionnelles, en accord avec la chronobiologie, associée à de l’exercice bien adapté et d’autres ajustements du style de vie, permet d’éliminer en premier les excès de graisse viscérale.
⇪ ✓ Ouvrages
🔵 Notes pour la version papier :
- Les identifiants de liens permettent d’atteindre facilement les pages web auxquelles ils font référence.
- Pour visiter « 0bim », entrer dans un navigateur l’adresse « https://leti.lt/0bim ».
- On peut aussi consulter le serveur de liens https://leti.lt/liens et la liste des pages cibles https://leti.lt/liste.
- A1 · qdml · The poor, misunderstood calorie (William Lagakos, 2012)
- A2 · ojj9 · FAT — Pourquoi on grossit (Garry Taubes, 2012)
⇪ ▷ Liens
Article créé le 2/09/2015 - modifié le 6/03/2026 à 10h04 • 9 147 visites




 9147
9147

